GB 12290—90 本标准参照采用国际标准ISO 5519—1978《水果、蔬菜及制品—山梨酸含量的测定》。 1 主题内容与适用范围 本标准规定了水果、蔬菜及制品中山梨酸的提取方法和提取物中山梨酸的两种测定方法。 本标准适用于水果、蔬菜及制品中山梨酸的测定。 2 原理 匀化样品,存在于试样中的山梨酸通过蒸汽蒸馏,可定量地蒸出。所得馏出物在铜催化剂的作用下使二氧化硫氧化以除去干扰,然后用紫外分光光度法测定山梨酸含量,或者通过铬酸氧化后用硫代巴比妥酸处理得到粉红色溶液,用分光光度法测定。 3 试剂和溶液 本标准所用试剂均为分析纯试剂,使用蒸馏水或相应纯度的水。 3.1 酒石酸,结晶状; 3.2 山梨酸标准溶液,0.01g/L: 准确称取0.100g山梨酸溶于10~12mL 0.1mol/L氢氧化钠溶液中,定量的移入1000mL容量瓶里,用水稀释至刻度。吸取上述溶液50.0mL置于500mL容量瓶中用水稀释至刻度。 3.3 氢氧化钙溶液:0.02mol/L; 3.4 铜催化剂溶液: 称取0.5g碳酸氢钠(GB 640)和0.001g硫酸铜(GB 665)(CuSO4·5H2O)用蒸馏水溶解并稀释至1L。 3.5 铬酸-硫酸溶液: 3.5.1 0.15mol/L硫酸溶液:取8.4mL比重1.84g/mL的浓硫酸(GB 625)加入水中,稀释至1L。 3.5.2 铬酸-硫酸溶液:称取0.05g重铬酸钾(GB 624)溶于90mL水,移入200mL容量瓶中,加入0.15mol/L硫酸溶液,用水稀释至刻度。 3.6 硫代巴比妥酸溶液: 称取0.500g硫代巴比妥酸溶于50mL水中。加入10mL 1mol/L氢氧化钠溶液,移至100mL容量瓶中,加入11mL 1mol/L盐酸溶液,用蒸馏水稀释至刻度。 该溶液不稳定,必须在配制后5h内使用。 4 仪器、设备 常用实验室仪器、设备。 4.1 分析天平:感量0.001g; 4.2 捣碎机或研钵; 4.3 电热恒温水浴; 4.4 蒸汽蒸馏装置,见下图: 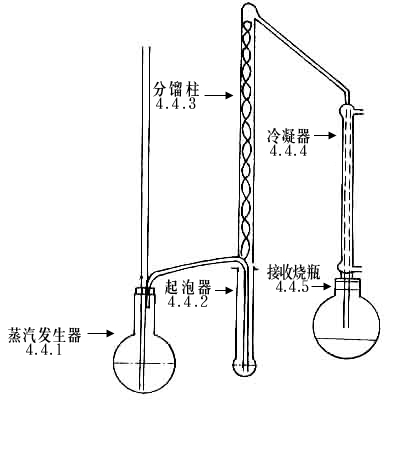
蒸汽蒸馏仪图 4.4.1 蒸汽发生器:烧瓶容量为1000、1500mL; 4.4.2 起泡器:玻璃管直径30mm,高270mm下部封闭,末端扩大为直径60mm的球体,试样放在球体内,供气管末端与起泡器底部之间距离为10mm。用电炉或火焰加热均可,若用火焰加热时,起泡器底部应放在一个具有孔径为40mm金属板的孔上,使火焰反射,避免试样焦化。控制加热使起泡器中试样的体积的蒸馏期间减少或增加的量不超过5mL。 4.4.3 分馏柱:直径20mm,高500mm的玻璃柱内装螺旋形100号不锈钢网,螺旋环间距15mm。 或是直径20mm,高600mm具有玻璃定心孔的分馏柱。 或是具有同等分馏功能的其他装置。 4.4.4 冷凝器:有效长度400mm,垂直放置,以保证蒸汽的冷凝和馏出物的完全冷却。 4.4.5 接收烧瓶:200、500mL容量瓶。 4.4.6 蒸馏装置效果检查:在正常蒸馏条件下,用20mL 0.1 mol/L乙酸溶液加入起泡器中,在15~20min内收集蒸馏液200mL,乙酸的回收率应达99.5%。 4.5 分光光度计:检测波长256nm或532nm。 5 分析步骤5.1 试样的制备 5.1.1 液体样品(汁、液、糖浆等)和粘稠样品(果酱、菜泥等),将样品充分混合后匀化。 5.1.2 固体样品(水果、蔬菜) 将样品切成小块,检去种子和果壳,取约40g,在捣碎机或研钵中(4.2)使其匀化。 冷冻的样品,首先在密闭容器中融化,将融化的液体与样品合并后匀化。 5.2 试样的分取 5.2.1 液体样品 吸取10.0mL试样(5.1.1)放到起泡器(4.4.2)里。或称取试样10g,精确至0.01g。 5.2.2 粘稠或固体样品 称取10g试样(5.1.1)精确至0.01g,放入起泡器(4.4.2)里,加水量至少需要淹没全部样品,摇匀,使其充分液化。若需要可将试样在水里浸泡1~2h。 5.3 蒸馏 将0.5g酒石酸(3.1)放进盛有试样的起泡器里,把起泡器与烧瓶(4.4.1)和冷凝器(4.4.4)连结,同时加热烧瓶和起泡器,进行蒸馏,保持起泡器内容物体积增减在 5mL以内。 5.3.1 对液体样品(5.2.1),收集蒸馏液于200mL的容量瓶(4.4.5)内,当达到刻度时,停止蒸馏。 5.3.2 对粘稠或固体样品(5.2.2),收集蒸馏液于500mL容量瓶(4.4.5)内,蒸馏液的体积至少比起泡器内容物体积大20倍。 5.4 测定 5.4.1 方法A:用紫外分光光度法测定 5.4.1.1 如果原产品含有大蒜、洋葱、韭菜的香精油时,为消除香精油的吸光度,用移液管取25mL蒸馏液(5.3)移入小蒸发皿中,加1.5~2.0mL的氢氧化钙溶液(3.3)使其呈碱性,在沸水浴(4.3)上蒸干,然后用蒸馏水溶解残渣使其恢复到原来的体积。 5.4.1.2 吸取10.0mL蒸馏液(5.3)或蒸干后重新得到的溶液(5.4.1.1) 置于 50mL锥形瓶内,加10mL铜催化剂(3.4),摇动,静置与空气接触几分钟。 以试剂空白作对照,于分光光度计(4.5)256nm波长处测定溶液的吸光度。 注:通常分取10.0mL,相当于200mg/L或kg,对于高含量的样品只取5.0或2.0mL用水稀释至10.0mL。 5.4.1.3 标准曲线的绘制 吸取山梨酸标准溶液(3.2)0.0、1.0、2.0、3.0、5.0、10.0mL分别置入50mL锥形瓶中,相应加入蒸馏水10.0、9.0、8.0、7.0、5.0、0.0mL使体积为10mL,所得溶液的浓度为:0、1、2、3、5、10mg/L的山梨酸,分别向每瓶中加铜催化剂 10mL。以试剂空白为对照,于分光光度计256nm波长处测定溶液的吸光度。以山梨酸的含量为横坐标,吸光度为纵坐标,绘制标准曲线。 5.4.2 方法B:分光光度法 5.4.2.1 如果原产品中含乙醇,吸取25mL的蒸馏液(5.3)移入小蒸发皿中,加1.5~2.0mL的氢氧化钙溶液使之呈碱性,在沸水浴上蒸发到原体积的一半,用蒸馏水冲洗皿,定量转移至25mL的容量瓶中,定容、摇匀。 如果原产品含(柑桔、大蒜、洋葱、韭菜的)香精油时,可按步骤5.4.1.1进行。 5.4.2.2 吸取10.0mL蒸馏液(5.3)或经处理制得的溶液(5.4.2.1)于25mL容量瓶中,加入4mL铬酸-硫酸溶液(3.5),放入沸水浴中10min。加4mL硫代巴比妥酸溶液(3.6),再置沸水浴中20min。溶液呈粉红色,取出放在冰水浴中冷却,用蒸馏水稀释至刻度。 同时按上述方法制备试剂空白溶液。 在30min内,以试剂空白作对照,于分光光度计532nm波长处测定溶液的吸光度。 5.4.2.3 标准曲线的绘制 配制2.0mg/L山梨酸标准液,用4体积水稀释1体积的标准溶液(3.2)。吸取该液0.0、2.0、4.0、
6.0、8.0、10.0mL分别置入6个25mL的容量瓶内,相应加入水10.0、8.0、6.0、4.0、2.0、0.0mL,使
体积至10mL,所得标准系列的浓度为0、0.4、0.8、1.2、1.6、2.0mg/L山梨酸。以下步骤按试样的测
定(5.4.2.2)进行。 以山梨酸的含量为横坐标,吸光度为纵坐标,绘制标准曲线。 6 分析结果表示6.1 计算方法和公式 6.1.1 液体样品 山梨酸含量以mg/L表示,按式(1)计算: | 

